
列島縦断AMR対策
事例紹介シリーズ
TOP > 列島縦断AMR対策事例紹介シリーズ > ファージ療法の現在地と展望~ファージが拓く感染症治療の可能性~
このコーナーでは、薬剤耐性(AMR)対策に関するさまざまな話題をご紹介しています。第28回で取り上げるのは、ファージ療法です。ファージ(正式名称:バクテリオファージ/Bacteriophage)は細菌に特異的に感染するウイルスで、近年、薬剤耐性菌などによる感染症の治療選択肢として注目されています。ファージ療法の実際や課題などについて、国立健康危機管理研究機構 国立国際医療センター 国際感染症センター・総合感染症科の早川佳代子先生にお話を伺いました。

早川佳代子(はやかわかよこ) 氏
国立健康危機管理研究機構 国立国際医療センター 国際感染症センター・総合感染症科 医長
2001年東北大学医学部卒業、2009年同大学院医学系研究科卒業、2009~2012年Wayne State University/Detroit Medical Centerを経て2012年より現職。2018年より総合感染症科医長。
創薬を目指す「固定化ファージ療法」とテーラーメイドの「個別化ファージ療法」
細菌内で増殖し、溶菌作用を発揮
ファージ療法とはどのような治療法なのでしょうか?
早川氏 ファージは細菌に感染するウイルスで、バクテリオファージとも呼ばれます。ファージは狙った細菌にくっついて中に遺伝子を入れ、細菌の中で増えて、最後に細菌を壊して外に出ます(溶菌)(図1)。この性質を利用したのがファージ療法です。
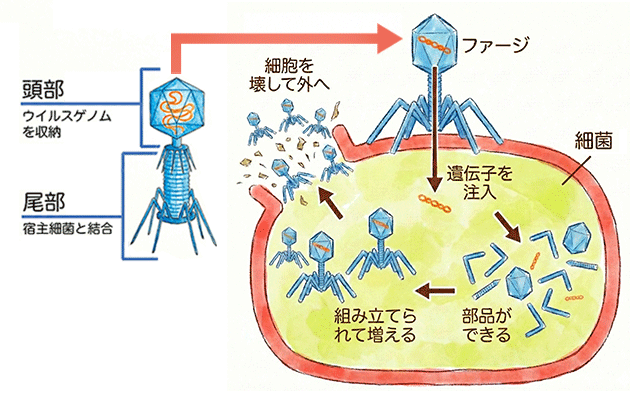
図1 ファージの構造と細菌に感染して壊す仕組み
現在、ファージ療法には世界的に大きく2つの流れがあります。1つは創薬、すなわちあらかじめ候補となるファージを選定して製剤化し、医薬品としての開発を目指す固定化ファージ療法です。もう1つは、患者から検出された細菌に合わせてファージを選び、テーラーメイドの治療を行う個別化ファージ療法です(表1)。いずれも細菌感染症、特に薬剤耐性菌などによる難治性感染症に対する治療選択肢として期待されています。

表1 固定化ファージ療法と個別化ファージ療法
ファージはヒトには感染しないのですか?
早川氏 しません。ファージはヒト細胞では増殖できないウイルスで、感染標的は細菌です。実際、「細菌あるところにファージあり」といわれ、両者ははるか昔から共生してきました。自然界にも広く存在し、表層海水では1mLあたり約107個ものウイルス粒子(多くはファージ)が含まれています。ヒトとも共生関係にあり、感染対象とする腸内細菌がひしめくお腹の中にもたくさん存在していて、ヒトの糞便1g中には109個前後のファージが認められます。特に病気などがない人でも日常的にファージと暮らしており、決して特殊なウイルスというわけではありません。
ファージ療法は、いつ頃から行われているのでしょうか?
早川氏 ファージとその溶菌作用が発見されたのは1910年代で、当初は東欧や旧ソ連圏で研究や臨床応用が進められました。その後、抗生物質の登場によってしばらく研究が停滞しましたが、2000年代以降、関連研究は増加し、近年は年間700~1,000報規模で報告されています。その背景として抗生物質の効かない菌が増えてきたこと、また、ファージの解析技術や安全性に関する検討が海外で少しずつ進んできたことなどが挙げられます。
抗菌薬との違いは、宿主域の狭さ
ファージは抗菌薬とどう違うのですか?
早川氏 最大の違いは、ファージは宿主域が非常に狭いということです。抗菌薬には「効く菌の範囲(スペクトラム)」があり、1菌種だけに完全に限定される薬は多くありません。例えば細胞壁合成を阻害する薬は、細胞壁をもつ細菌に効きやすい一方で、菌種や耐性の有無によって効き方は変わります
これに対し、ファージは「特定の黄色ブドウ球菌の中の、特にこの菌株だけに感染する」というように、感染する対象が極めて限られています。この宿主域の狭さがファージの特徴で、だからこそ抗菌薬よりもテーラーメイドに寄せた治療が可能になるといえます。
そうすると、宿主となる細菌が完全に特定されなければ、ファージ療法を行っても意味がないのでしょうか?
早川氏 固定化ファージ療法、すなわち医薬品開発につなげようという場合は、患者ごとに菌株レベルで完全一致させるという点では個別化ほど厳密ではありません。例えば糖尿病による足感染であれば、起因菌として多い菌を洗い出し、「この菌とこの菌にマッチすれば効果が期待できるだろう」と考えて、複数のファージを選び出す、というアプローチが取られます。ただし、ファージは宿主域が狭いため、すべての症例で菌にマッチするとは限らず、治療効果にばらつきが出やすいことは否めません。なぜなら菌名はマッチしていても、菌株によって効く場合と効かない場合があるからです。
一方、個別化ファージ療法では菌に完全に合わせていきます。個々の患者で標的となる菌を採取し、その菌を用いて菌株レベルで溶菌活性を示すファージがないか、探す作業を行います。完全にテーラーメイドの治療なので、原則として菌とファージがマッチしなければ治療は成立しないということになります。
逆に、菌とファージがマッチすれば大きな効果が期待できそうですね。
早川氏 個別化ファージ療法の奏功例としてよく知られるのが、パターソン症例です。2015年11月、旅先で急性膵炎を起こした米国人のパターソン氏は、ほぼすべての抗菌薬が効かない多剤耐性アシネトバクター感染症を併発し、昏睡状態に陥りました。しかし研究者だった夫人の提案がきっかけで、2016年3月からファージ療法を行った結果、全身状態が改善し、8月には退院できるまでに回復しました。効果が期待できる抗菌薬が乏しい状況で、当時の状況からは救命が危ぶまれていた症例にもかかわらず、静脈注射を含む個別化ファージ療法が実施され奏功した米国の最初期の報告として知られています。
溶菌活性を調べることでファージを選定
個別化ファージ療法ではその都度、受容体を特定するのでしょうか?
早川氏 いえ、受容体を調べるのではなく、もっと迅速に、細菌とファージを組み合わせて溶菌活性があるかどうかを調べます。問題となる細菌をファージの研究機関に提出し、ファージライブラリの中からその細菌を溶菌できるファージがないか、スクリーニングが行われます。ライブラリに適合するものがなければ、生活排水などの環境の中から探すこともあります。
先ほどのパターソン症例では、溶菌活性を示した複数のファージが選定・投与され、その後ファージに耐性菌が出現すると、別の複数のファージの選定・投与が行われ、最終的にアシネトバクター耐性菌の消失が認められた、という経緯があります。
ファージはどのように投与するのですか?
早川氏 ファージを溶液として調製して投与しますが、投与経路はさまざまです。病気が起きている場所に局所投与する方法のほか、静脈注射や経口、また吸入も行われています。パターソン症例では、ドレナージ(排液)のために入れていたカテーテルからファージを腹部の感染局所へ投与したほか、敗血症を併発していたため静脈内投与も行われました。ファージの投与自体に手技として特段の難しさはなく、さまざまな投与経路が報告されています。ただし、どのルートでも一律に適用できるというより、病態や感染部位に応じて選択されます。
どの投与経路が最適か、ある程度わかっているのでしょうか?
早川氏 これまでの報告を見る限り、病変部に直接投与する方がより効果的である可能性がありますが、経路間で一概に比較できるだけのデータはまだ十分ではないのではないかと思います。抗菌薬の開発では、PK/PD(薬物動態/薬力学)という指標に基づいて適切な投与量や投与間隔が設定されます。一方、ファージはその性質上、PK/PDを抗菌薬と同じ枠組みでそのまま適用するのが難しく、データもばらつきが出やすいことが指摘されています。最適な投与経路はあくまで患者の病態による、ということになるかと思います。


